不仅仅是免疫细胞
对于一些人来说,当他们想到巨噬细胞时,他们会想象一个真实的生命微观版本的吃豆人在他们的身体周围运行,摄入任何微生物入侵者。

虽然这是过去100年来围绕这种免疫细胞的中心法则 - 但越来越明显得是这不是事实的全部。在过去的十年中,已发表的许多论文中确定了由不起眼的巨噬细胞进行的新功能和过程。更重要的是,我们发现组织内的巨噬细胞具有器官特异性功能。例如,巨噬细胞被证明有助于脾脏和肝脏中的铁循环(Theurl et al.2016),脂肪组织中的热生成调节(Nguyen et al.2011)以及心脏中的电传导(Hulsmans et al.2017)。
您是否想告诉我这些微小的白细胞在多任务处理方面比我更好? 嗯,是的。 这正是我要告诉你的。
哈佛医学院的一组研究人员在《细胞》杂志上发表的一项研究表明,心脏内的巨噬细胞在促进稳态心脏的电传导方面起着重要作用。通过将心脏研究技术(如体表和遥测 ECG 监测)与免疫学技术(如流式细胞术和转基因小鼠的使用)相结合,他们发现了心脏巨噬细胞的秘密生命。
巨噬细胞的彩色扫描电子显微照片。 图片来源:NIAID
心脏巨噬细胞与邻近的心肌细胞形成含有 Cx43 的间隙连接
心肌细胞或心脏细胞通过间隙连接彼此连通。间隙连接允许相邻细胞之间的小分子和离子的传输,在心脏中促进组织的同步收缩和随后心跳的产生。连接蛋白(Cx)蛋白是这些细胞间通道的螺母和螺栓,有各种异构体。特定异构体 Cx43 已被证明可连接心肌细胞与非心肌细胞。
通过流式细胞术和RNA测序,研究小组发现房室结内的巨噬细胞显示 Cx43。为了证明巨噬细胞使用Cx43连接蛋白与邻近的心脏细胞形成间隙连接,他们使用电子显微镜仔细观察细胞。这使得研究小组能够直观地看到两种细胞类型之间的直接膜接触,表明可能的细胞间通信。
巨噬细胞影响房室结传导
为了研究细胞 - 细胞通讯是否通过 Cx43 连接发生,该团队使用了功能丢失实验,他们在房室结节内的巨噬细胞中删除了 Cx43。为此,他们使用了三苯氧胺诱导系统,通过向转基因小鼠注射三苯氧胺,他们可以特异性地删除心脏巨噬细胞中的 Cx43。为了测量移除cx43连接对房室结传导的影响,他们使用一个插入右心房和心室的 Millar Mikro-Tip 8电极导管(EPR-800)结合体表心电图/心电图记录进行一项在体电生理学(EP)研究。
使用连接到动物用生物电放大器和 PowerLab 的皮下电极测量并记录体表的 ECG,随后使用 LabChart Pro 中的 ECG 模块分析数据。这使研究小组能够以不同的方式刺激心脏,并测量对心脏电活动的后续影响。比较对照和转基因小鼠的结果,他们发现在没有 Cx43 的情况下,房室结传导受损,表明心脏巨噬细胞可以影响心脏的电传导。
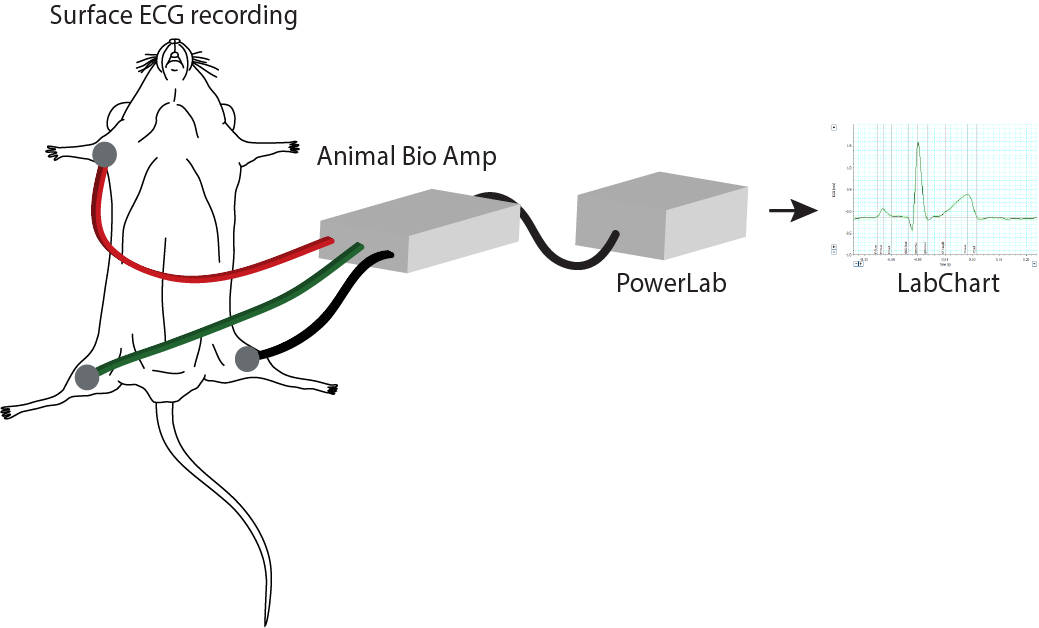
简化了体表 ECG 记录的设置。 连接到 PowerLab 的动物用生物电放大器放大了信号,并在 LabChart 中进行分析。
心电图遥测显示缺乏巨噬细胞的小鼠心脏跳动不规则
下一步,研究小组想研究,如果消耗常驻巨噬细胞种群,是否会对房室结传导产生类似的影响。他们通过基因改造小鼠来达到白喉毒素(dt)诱导系统,给药后会导致巨噬细胞(和其他骨髓细胞)的消耗。为了监测对心脏的后续影响,他们将植入式心电图遥测设备(DSI)置于腹部的第二导联位置。这样能在8天内连续记录 ECG 数据,并使用 LabChart 软件分析数据。有趣的是,在单剂量DT的24小时内,所有小鼠都出现一级房室传导阻滞,并超时地进展到三度阻滞。心房和心室之间的传导受损时发生房室传导阻滞。 临床上,房室传导阻滞会加重诱发病情,例如心力衰竭。
本研究中使用的心脏和免疫学研究技术的独特整合揭示了巨噬细胞在促进心脏电传导及其潜在的心脏病诱发中所起的作用。多年来,我们将我们的身体划分为不同的生理系统,由具有不同功能的不同细胞类型组成。然而,通过这样的研究,我们开始理解这些所谓的“不同”细胞类型的惊人适应性和协同性,并发现这些系统是如何真正交织在一起的。
有兴趣在您的研究中使用上述某些技术?
查看以下页面获取更多信息:
生物电遥测基础系统 (Biopotential Telemetry Foundation System)
小动物遥测植入子
更多详细信息,请访问 Macrophage – the new miracle cell? How white blood cells help maintain a healthy heart beat
References
- Nguyen KD, Qiu Y, Cui X, Goh YP, Mwangi J, David T, et al. Alternatively activated macrophages produce catecholamines to sustain adaptive thermogenesis. Nature. 2011;480:104-108.
- Theurl I, Hilgendorf I, Nairz M, Tymoszuk P, Haschka D, Asshoff M et al. On-demand erythrocyte disposal and iron recycling requires transient macrophages in the liver. Nat Med. 2016;22:945-951.
- Hulsmans M, Clauss S, Xiao L, Aguirre AD, King KR, Hanley A, et al. Macrophages facilitate electrical conduction in the heart. Cell. 2017;169:510-522.