什么是离体器官研究 - 为什么要开展该研究?
顾名思义, 离体器官研究 涉及从体内取出一个器官,并为实验目的维持其生理功能。
这项技术在研究器官对各种刺激(药物或化学物质)的生理和药理反应时非常有用,不受其他系统过程的干扰。
在过去 100 年中,已经使用各种离体器官技术研究了诸如心脏、肝脏、肾脏和肺等器官,包括全器官、部分器官、灌注器官和非灌注器官方案。
因此,如果您尚未亲自尝试这项技术,则有必要了解离体器官研究对您研究实验有益的三大原因!
离体器官研究的三大主要优势
1. 清晰和快速
通常,当生理条件发生变化时,身体相应地调节以维持全身体内平衡,这可导致许多生理参数同时变化。通过移除器官并在受控环境中进行研究,记录的反应不受身体影响, 而这些影响可能是不可见的或未知的。这意味着,涉及到分析时,可以相对简单快捷的方式获得更清晰、更明确的结果。
此外,还有一个额外优势,即能够记录实验过程中可能发生的任何目视观察,例如颜色或形态变化,从而获得额外定性数据。
2. 全面环境控制
离体器官系统允许控制器官环境,例如固定或改变缓冲液或灌注液成分、温度、压力、流量和氧合作用,这些因素通常都受体内平衡控制。这意味着能够创建和维持不同的病理生理条件,例如缺氧、低/高血压或毒性(药物)条件,从而避免正常体内平衡功能干扰。

使用精确可靠的监控和记录工具可以轻松控制离体器官环境,例如我们的温度和 pH 套件、O2 & CO2 套件以及 Transonic 流量探针和流量传感器,这些工具可以添加到我们的任何一个 离体器官系统。
3. 灵活性和直接测量
最后,借助离体器官系统,可以根据研究需要灵活扩展或减少实验方案的复杂性。此外,由于它是一种有创方法,可以直接在器官上放置传感器或电极,以提高测量精度和准确度。
相关内容:如何设置一个典型的离体灌注啮齿动物肝脏 (IRPL) 实验。
ADInstruments 的优势
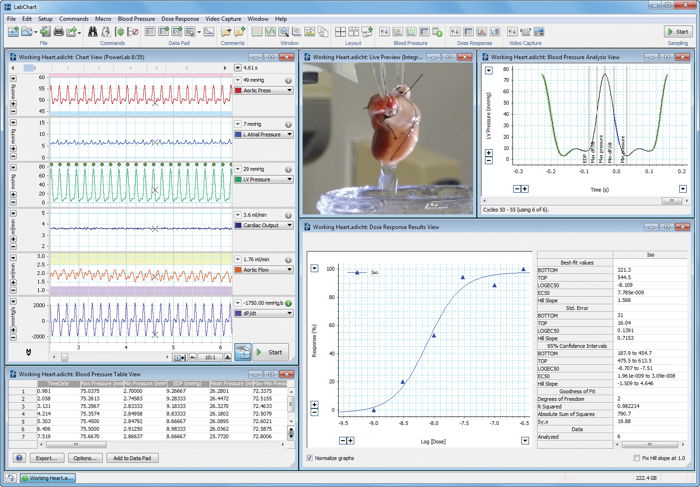
ADInstruments 为您提供使用同一个记录和分析平台测量和分析来自离体器官标本的各种不同信号的机会。借助我们的 PowerLab 数据采集系统和 LabChart 分析软件,您可以在同一款软件中同时记录不同信号,并轻松识别记录信号之间的关系。
例如,如果您想观察某种特定药物对离体心脏的药理作用,您可以给心脏施用不同浓度的药物,同时测量心脏参数的任何变化,例如心率 (ECG)、收缩性(使用 Bridge Amp(桥式放大器) 和 张力传感器)或 血压。然后,利用 LabChart 的量效模块,您可以快速自动推导出相应的量效曲线,以自动计算 EC50 值。
离体灌注啮齿动物肝脏 (IPRL)
多年来,ADInstruments 一直与 Radnoti 专家合作,创造离体组织器官研究所需的精密、优质玻璃器皿,为离体心脏实验提供各种解决方案,包括 Langendorff 系统和 工作心脏系统。关于最新合作产品,我们创建了一套离体研究肝脏的解决方案。IPRL 由 Claude Bernard 于 1855 年首次报道,当前仍然是一种可靠且普遍采用的再灌注模型,应用领域包括:
- 肝脏作用研究
- 肝损伤评估
- 肝脏保存和移植研究
- 肝病研究:肝炎、肝硬化、肝癌、肝功能衰竭
- 肝脏与胰岛素和激素调节的关系

我们的最新离体器官产品:
离体灌注啮齿动物肝脏基础系统
一种用于灌注离体啮齿动物肝脏以维持其肝功能的玻璃仪器基础系统。它具有用于数据收集和分析的采集硬件和软件,包括压力、流量和温度。
Radnoti 离体啮齿动物肝脏/肾脏仪器
已经有 PowerLab 和 LabChart 了吗?那么这就是您的解决方案。一种设计用于维持离体啮齿动物(小鼠或大鼠)肝脏或肾脏标本功能的玻璃仪器,并在灌注回路中测量多达两个灌注压力。
想要开始使用我们的离体肝脏系统,但不知道从哪里开始? 在进行 IPRL 实验时,请查看我们关于重要注意事项的简要指南。
相关内容:帮助解决(离体)心脏问题:心血管药理学研究的便捷性 & 灵活性
参考文献
Yeh T., Wechsler A.S. (1998) The Isolated Organ in Research. In: Troidl H., McKneally M.F., Mulder D.S., Wechsler A.S., McPeek B., Spitzer W.O. (eds) Surgical Research. Springer, New York, NY
Shatoor, Prof. Abdullah & Al-Hashem, Professor Fahaid & Elkarib, Abbas & Sakr, Hussein & Alkhateeb, Mahmoud. (2012). EC50 of adrenaline-atenolol: Functional agonist assay using Langendorff isolated rabbit heart tethered to PowerLab data acquisition system. African journal of pharmacy and pharmacology. 6. 1092-1098. 10.5897/AJPP12.123.
Bessems M et al. 2006, The isolated perfused rat liver: standardization of a time-honoured model, Laboratory Animals.