我们采访了 Aaron Phillips 博士,了解他在《自然》杂志上发表的有关人工纠正脊髓损伤后血流动力学不稳定的文章,以及 Kaha 遥测技术如何帮助他表征多种动物模型的心血管调节。

Aaron Phillips 博士是卡尔加里大学副教授兼 RESTORE.network 主任。 出于对神经系统和心血管系统之间复杂相互作用(包括导致临床疾病的异常相互作用)的热情,Aaron的研究重点是为患有神经系统健康问题的人开发新的疗法。
在本文中,我们详细介绍了人工神经压力感受反射的发展,这是一种旨在人工纠正脊髓损伤后血压的装置,以及 Kaha SNA 和压力植入子在表征多种动物模型的心血管调节方面所发挥的作用。Aaron 向我们介绍了他在《自然》杂志上发表的论文: Neuroprosthetic baroreflex controls haemodynamics after spinal cord injury, 以及他与 Gregoire Courtine 副教授共同领导的 Longitudinal interrogation of sympathetic neural circuits and hemodynamics in preclinical models .
创伤性脊髓损伤造成的衰弱效应是众所周知的。 除了药物和康复之外,新的治疗技术还探索对受损神经中枢进行电刺激以挽救肌肉控制。 Phillips实验室利用这项技术来解决脊髓损伤的一个鲜为人知的症状—血流动力学不稳定。 设计一种复杂的设备来电刺激负责维持危及生命的不稳定血压的神经中枢。
“脊髓损伤后的心血管不稳定实际上分为两个阶段,” Aaron说。 “受伤后 24 小时内是急性期,然后是慢性期。 在这个急性阶段,会出现一种叫做神经源性休克的现象,它是交感神经系统的严重抑制,血压非常低。 它会阻止脊髓的愈合。 它与神经损伤有直接关系。大约百分之五十的损伤发生在最初的创伤之后,即神经源性休克期间,此时血流不足以治愈脊髓。”
血流动力学不稳定,即身体无法维持一致的血流和压力,发生在脊髓损伤的慢性阶段。
这种不稳定会导致反复低血压发作; 增加卒中和心脏病的风险,同时严重影响脊髓损伤的恢复。尽管可以使用药物治疗,但它们会增加并发症的风险,并且往往依从性较差。Aaron和他的团队希望找到一种能够直接针对受伤系统、高效且副作用可忽略不计的解决方案。

过去五年来,开发解决脊髓损伤后血压不稳定的新方法一直是Phillips实验室的重点。
血流动力学不稳定的临床前模型
在开发血流动力学不稳定的治疗方法时,Phillips实验室确保他们深入了解交感神经系统的参与。
“我的理念是,在尝试开发新东西之前了解生物学机制至关重要,”Aaron说。 “我认为,如果不深入了解潜在的生物学机制,要了解如何最好地优化干预措施是非常具有挑战性的,甚至可能是不可能的。”
Squair 等人探索的第一个临床前模型是一只酪氨酸羟化酶 (TH)-Cre 大鼠,其上胸脊髓 (T3) 出现临床相关挫伤。 Phillips小组将调节血流动力学的下行通路的损伤可视化。 通过病毒注射带有基因表达荧光标记的神经元,可以标记从头端腹外侧延髓(RVLM)向下投射到脊髓的神经元。 这很重要,因为 RVLM 是负责激活交感系统控制心血管功能的大脑区域。 这使得Aaron和他的团队能够追踪压力反射从大脑到脊髓的交感神经通路。
该模型显示损伤下方神经元的交感兴奋性突触几乎完全减少。
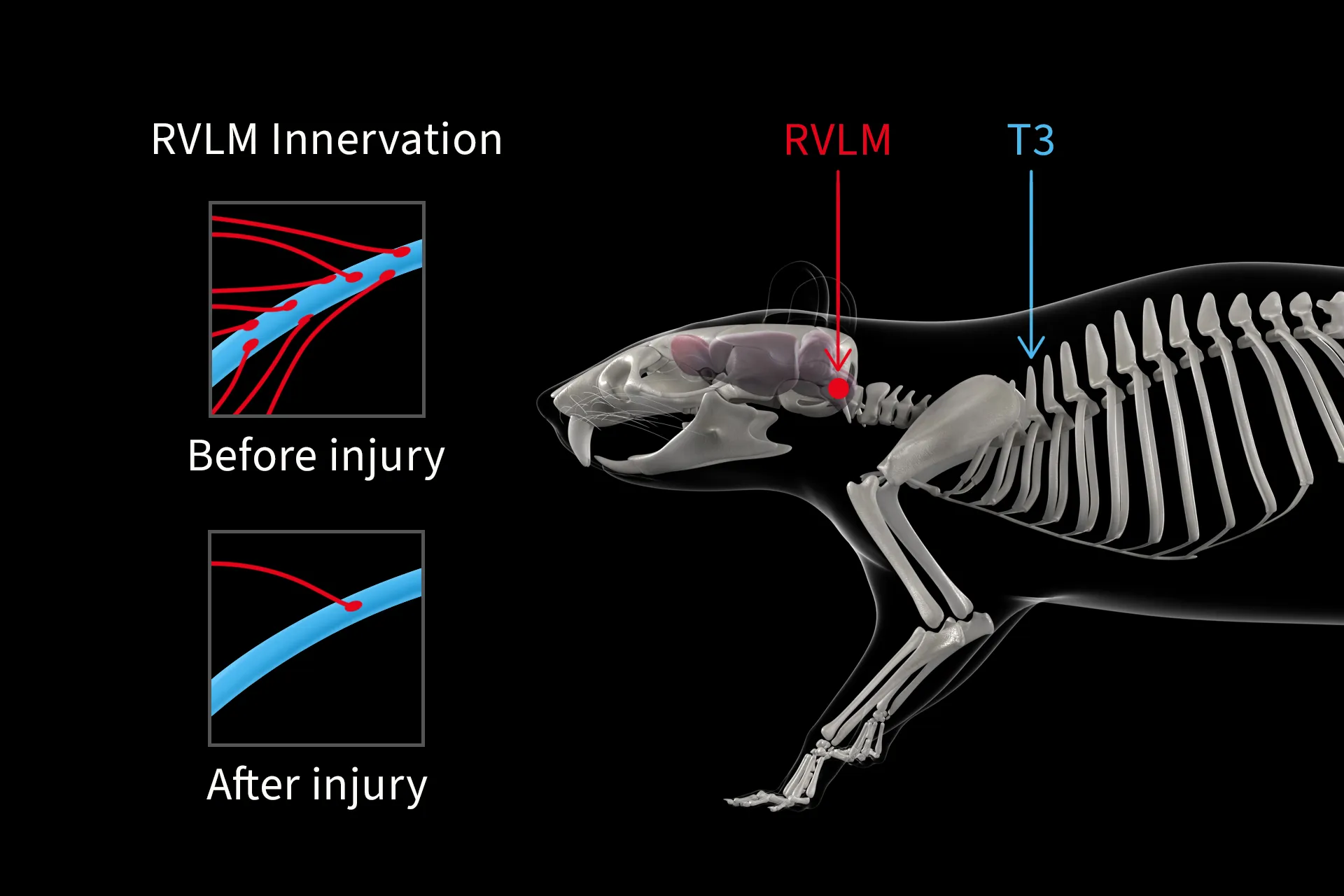
为了描述交感心血管控制的缺乏如何影响大鼠模型的血流动力学,Phillips研究小组植入了Kaha SNA 和压力植入子用于长期、同时测量交感肾神经活动和动脉血压。
“这是一个很棒的工具,” Aaron说。 “首先, 它为我们提供了必要的数据,以便深入了解自由活动动物的日常生活中脊髓损伤后心血管和交感神经系统随时间的变化情况。它使我们能够了解这些系统如何随着时间的推移对扰动做出反应。”
“这一见解为我们提供了证据,以确定大鼠对直立挑战具有抵抗力,这是表征模型的关键信息。”
“它还让我们了解交感神经系统和心血管系统是如何相互作用的。”
Phillips小组在中腹部下方开发了一种全新的临床前负压室,将血液拉向动物的后肢。 这种新装置首次允许在脊髓损伤的临床前模型中研究直立性低血压。Kaha植入子证实,这种直立挑战会导致与脊髓损伤患者的临床“倾斜测试”中观察到的相同的血流动力学变化。

未损伤的大鼠在快速恢复之前会经历短暂的低血压,而脊髓损伤的大鼠则经历与腔室压力线性相关的持续低血压。
刺激血流动力学热点
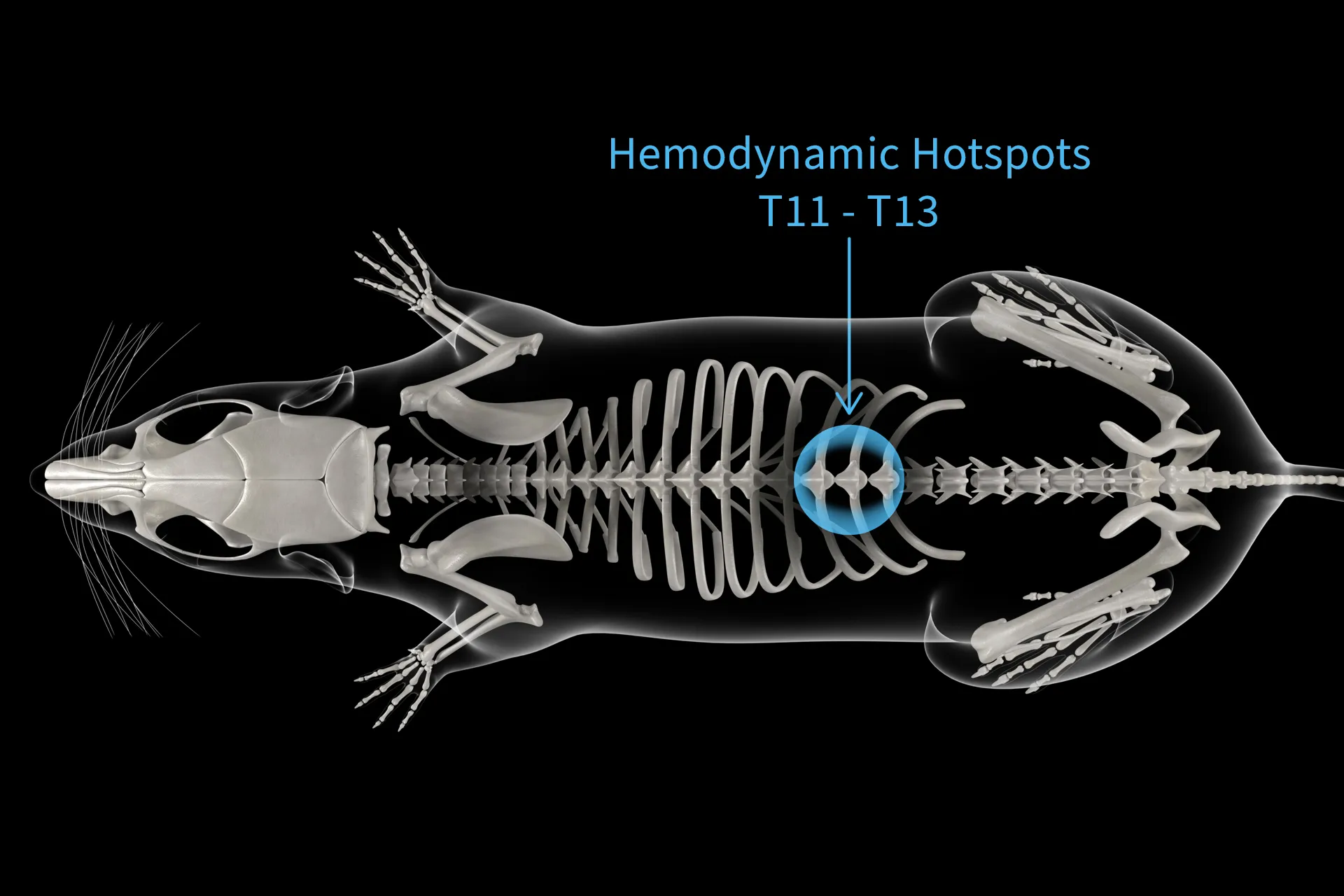
研究小组利用内脏交感神经节(一组神经节纤维,其中包含投射到参与血压调节的血管的神经元)的逆行追踪来确定刺激的最佳靶点。对这些纤维的逆行追踪显示, 参与血压控制的脊髓神经元浓度在低胸区(T12 左右)达到峰值。
当对每个脊柱节段施加硬膜外刺激后根 (TESS) 时, Kaha 遥测显示刺激 T11-13 期间血压升高。这些血流动力学热点与逆行追踪的神经元密度相关。 据确定,应用于 T11-13 的 TESS 主要招募后根中的大直径传入纤维来执行这种升压反应。 在观察到这些传入投射的消融与 TESS 期间的升压反应抑制相关之后,这一点得到了证实。
“这项工作涉及的所有步骤都不是微不足道的,但病毒追踪是最困难的方面之一,特别是在脊髓内,”Aaron说。 “我们花了很多时间进行反复试验,寻找方法,以便我们能够了解血压和交感神经系统响应硬膜外刺激而激活所必需的神经元间活动。 我们为此花费了大量的时间和资源。”
在此处阅读有关Philips小组用于预测神经募集的计算模拟的更多信息 »
模仿现实的刺激
为了为脊髓损伤后血流动力学不稳定提供长期解决方案,Aaron和团队开始尝试模仿正常交感神经活动的方案,在脊髓损伤部位以下复制这种活动。Kaha SNA 和压力植入子 是本次测试的重要组成部分,随着试验的进展,不断提供有关交感神经和血流动力学活动的实时信息。
“重要的是不仅仅能够在动物被处死后的一次急性准备中测量这些类型的东西,”Aaron说。 “描述任何类型的伤害或干预随着时间的推移事情如何发生和进展是至关重要的。 这是确定事情是变得更糟还是变得更好的最佳方法。 市场上没有其他产品可以实现这些并发方法。 我们已经使用它们很多年了。”
制作了电子硬脑膜 (e-dura) 刺激器并将其植入脊柱,以针对 T11-13 脊柱节段的后根(血流动力学热点)。 记录延髓头端腹外侧神经元的活动表明,TESS 协议有效地模仿了自然交感神经环路激活的空间序列、频率内容和时间分布。 使用硬膜外刺激,Aaron和团队创造了一种人工神经压力感受反射,能够在发生神经源性休克的损伤急性期和体位动作期间稳定先前不稳定的血流动力学。
转化的第一步
E-硬脑膜植入物经过放大以适应非人类灵长类动物的解剖结构。 在 T3 发生急性、完全性脊髓损伤后,他们对 TESS 的升压反应被绘制出来。 与啮齿类动物一样,血流动力学热点存在于下胸段脊髓中。 这些非人类灵长类动物的血压是用Millar压力导管记录的; SNA 活动未使用遥测技术进行记录。 受伤后压力立即升高,随后出现严重低血压,这与在人类身上观察到的模式相同。
持续的TESS能够暂时缓解血压,但是,这种情况在几次心跳后就停止了。 利用临床级无线植入式脉冲发生器,Phillips小组能够调整他们的闭环系统,以与非人类灵长类动物的生理数据保持一致。 一旦校准,人工神经压力反射立即使血压正常化,并稳定受试对象先前不稳定的血流动力学,不受神经源性休克和直立挑战的影响。
转化研究造福患者生活
在研究的最后阶段,Phillips研究小组研究了他们的治疗对患有慢性、功能完整的颈脊髓损伤的人的疗效。 由于受伤,患者出现了使人衰弱的直立性低血压。 如果这种治疗方法确实对人类有效,那么将会带来明显的好处。
通过手术将桨式电极阵列植入 T10 和 T11 下方,以最好地瞄准临床前模型中确定的血流动力学热点。 TESS 诱导强烈的升压反应,使去甲肾上腺素的循环水平正常化,并增加交感神经活动,证实了交感神经环路的激活。 当遇到“倾斜台”的挑战时,只需对 TESS 振幅进行模拟闭环滴定即可抵消直立应力并保持血流动力学稳定性。
随着TESS的长期实施,患者能够结束血流动力学不稳定的药物治疗,参与垂直运动康复,并彻底解决直立性低血压。
“在研究中,你经常会收集大量数据,直到所有数据都经过分析并显示出统计显著性后,你才能知道你的实验是否有效,”Aaron说,“但这只是有效的 - 当你打开它时,你可以用肉眼看到它。它每次都能稳定血压,它适用于跨物种,适用于急性和慢性环境; 它就是有效的。”
下一个是什么? 对于人工神经压力反射来说,旅程才刚刚开始。 它正快速走向临床研究并在世界各地进行。 “能够发现如此强大的东西真是太有意义了,”Aaron说。 “我们在这篇论文中合作的 Courtine 小组在瑞士对患者进行了一些手术。 我能够亲自参加这些活动,而且它一直在发挥作用。 我们在手术室里都击掌了。”
“我不想以任何方式夸大它,但它正在产生巨大的影响。 我们正在与一家名为 ONWARD MEDICAL 的上市公司合作,该公司完全致力于通过关键临床试验将这种疗法推向社区,我们已向该公司授予了我们的专利许可,并且他们与 Christopher 和 Dana Reeves 基金会以及美国军方 (DARPA) 等团体合作,”Aaron 说,“这个领域有大量的能量和加速力,可以将这种疗法带给社区。”
“现实情况是,将其推向社区的关键步骤现在正在发生。 我们在卡尔加里又植入了两名患者,我们正在验证手术方法和反应。 与 Courtine 博士一起在瑞士又进行了几次活动。 ONWARD 的该方法获得 FDA 突破性认定。 我们现在正在做这个。 ”
聆听 Aaron Phillips 博士在我们的网络研讨会上讨论这项研究:理解神经血流动力学控制的下一代技术»
欲了解更多信息,请参阅《自然》杂志上发表的这些文章:
Squair, Jordan W., et al. “Neuroprosthetic Baroreflex Controls Haemodynamics after Spinal Cord Injury.” Nature, vol. 590, no. 7845, 2021, pp. 308–14. https://doi.org/10.1038/s41586-020-03180-w
Soriano, Jan Elaine, et al. “Longitudinal Interrogation of Sympathetic Neural Circuits and Hemodynamics in Preclinical Models.” Nature Protocols, vol. 18, no. 2, Nature Portfolio, Nov. 2022, pp. 340–73. https://doi.org/10.1038/s41596-022-00764-w
其它资源
使用 Kaha Sciences 遥测技术的四种心血管应用 »
SmartPad 产品功能 – Kaha Sciences »

Aaron Phillips, Ph.D.
Aaron Phillips博士是卡尔加里大学的副教授。 出于对神经系统和心血管系统之间复杂相互作用(包括导致临床疾病的异常相互作用)的热情,Aaron的研究重点是为患有神经系统健康问题的人开发新的疗法。
